
¿Qué es la nomenclatura química?
La nomenclatura química es el término que se da a la denominación de los compuestos. Los químicos usan reglas específicas y «convenciones» para nombrar a los diferentes compuestos.
Esta sección está diseñada para ayudar al alumno a revisar algunas de esas reglas y convenciones. En química, se conoce como nomenclatura (o nomenclatura química) al conjunto de normas y pautas que se deben de seguir para nombrar o escribir las fórmulas de compuestos químicos de forma correcta y perfectamente entendible.
Dependiendo de los elementos que los componen y de la proporción de los mismos, se nombran de una u otra forma, siempre atendiendo al organismo de autoridad que dicta estas pautas, la IUPAC.
La importancia de la nomenclatura química radica en la posibilidad de nombrar, organizar y clasificar los diversos tipos de compuestos químicos, de manera tal que solamente con su término identificativo se pueda tener una idea de qué tipo de elementos lo componen, su naturaleza y su posible reactividad
En la antigüedad, existían tres sistemas de nomenclatura química:
- Sistema estequiométrico o sistemático (IUPAC): Nombra los compuestos en base al número de átomos de cada elemento que forman su molécula básica, utilizando prefijos multiplicadores.
Por ejemplo: el compuesto CO₂ se llama Dióxido de Carbono.
- Sistema clásico o tradicional: Emplea diversos sufijos y prefijos (como “-oso” o “-ico”) según la valencia de los elementos del compuesto.
Por ejemplo: el compuesto CO₂ se llamaba Óxido Carbónico.
(Ésta nomenclatura se desaconseja por la IUPAC, sólo se aceptan algunos nombres vulgares)
- Sistema Stock: El nombre del compuesto incluye en números romanos y entre paréntesis el número de oxidación de los átomos presentes en la molécula básica del compuesto.
Por ejemplo: el compuesto CO₂ se llama Óxido de carbono (IV).
(Actualmente, ésta nomenclatura como tal no se utiliza, ya que se ha ido sustituyendo por la nomenclatura de composición).
Ésta nomenclatura de composición a su vez, se divide en función de si se indica el número de oxidación o el número de carga como veremos en detalle más adelante.
Además, la nomenclatura y formulación química varía dependiendo de si se trata de compuestos orgánicos o inorgánicos.
Nomenclatura en Química Orgánica
El buen estudiante de química debe considerar memorizar los prefijos de al menos, los primeros diez compuestos orgánicos:
Prefijo según el número de carbonos:
1 met-
2 et-
3 prop-
4 but-
5 pent-
6 hex-.
7 hept-
8 oct-
9 non-
10 dec-
Nomenclatura en Química Inorgánica
La nomenclatura en química inorgánica incluye las siguientes familias:
Óxidos Ácidos
Óxidos Básicos
Hidruros
Hidruros Metálicos
Hidruros No Metálicos y Combinaciones del Hidrógeno con grupos 16 y 17
Iones Heteropoliatómicos
Hidróxidos
Sales Volátiles
Sales Neutras
Peróxidos Inorgánicos
Superóxidos
Oxoácidos
Ácidos Polihidratados
Oxosales
Derivados de Oxoácidos
Tioácidos
Peroxoácidos
Tipos de Nomenclatura en la Actualidad
- Tradicional (no podemos obviarla dado el número de publicaciones que la utilizan)
- Composición (con número de carga o de oxidación(antigua Stock))
- Sistemática (con prefijos multiplicadores)
Nomenclatura Tradicional
La nomenclatura tradicional contiene el nombre que identifica a una sustancia química, pero que no ha sido obtenido por aplicación de las reglas sistemáticas de la nomenclatura.
Existe un error muy común en considerar que la nomenclatura tradicional, aún se acepta en el Libro Rojo de la IUPAC, pero no es así. Lo que ocurre es que se aceptan algunos nombres vulgares para oxoácidos y oxosales.
Es muy popular y conocida por distinguir entre los compuestos conociendo el número de valencia de sus átomos, empleando así los añadidos per–ico, hipo–oso, -oso, -ico.
Se trata, sin embargo, de una nomenclatura en desuso, lentamente sustituida por la IUPAC, y que sobrevive meramente por historia, dado el gran número de publicaciones antiguas que la utilizan.
Nomenclatura Sistemática
La nomenclatura IUPAC o Sistemática es una de las reglas para nombrar compuestos inorgánicos más usadas en la actualidad. Esta consiste en nombrar los compuestos empleando prefijos griegos, los cuales nos indica el número de átomos presente en cada elemento involucrado en un compuesto dado.
Nomenclatura de Stock
Nomenclatura Sistemática STOCK. Este tipo de nomenclatura inorgánica consiste en nombrar los compuestos empleando números romanos para indicar los estados de oxidación de alguno de los elementos que forma parte de dicho compuesto. Estos números romanos se colocan al final del nombre específico.
Nomenclatura IUPAC
La IUPAC (en inglés, International Union of Pure and Applied Chemistry, es decir, Unión Internacional de Química Pura y Aplicada) es la organización internacional dedicada a establecer las reglas universales y que ostenta la autoridad absoluta en materia de nomenclatura química.
Su sistema, propuesto como un sistema simple y unificador, se conoce como nomenclatura IUPAC y aporta las mejores estrategias y pautas oficiales a seguir a la hora de nombrar compuestos.
El buen químico deberá de estar atento a todas las últimas actualizaciones de esta organización para que su forma de nombrar no quede obsoleta. La última gran actualización se realizó en el año 2005.
Nomenclatura de Composición
Los nombres de composición indican únicamente la cantidad de átomos de cada elemento en el compuesto. Dan poca información de cómo se distribuyen los átomos en la molécula.
Nomenclatura de Composición con números de carga
Esta nomenclatura es muy parecida a la antigua de Stock y sólo se aplica a compuestos con carácter iónico real, es decir, que formen auténticos iones.
Nomenclatura de Composición con números de oxidación
Idéntica a la antigua nomenclatura de Stock.
¿Cómo se nombran los diferentes compuestos químicos?
Cuando se forman compuestos, es importante saber algo sobre la forma en que los átomos reaccionan entre sí.
Oxidación-Reducción
Uno de los modos más importantes en que los átomos y/o las moléculas reaccionan entre sí es la reacción de oxidación/reducción. Las reacciones de oxidación/reducción son los procesos de perder y ganar electrones respectivamente.
Recuerda, «Sé positivo, pierde un electrón y oxídate»
Si pierde electrones se oxida, si gana electrones se reduce.
Los números de oxidación se asignan a los átomos y compuestos como un modo de decir a los científicos dónde están los electrones en una reacción. A menudo se le denomina «carga» en el átomo o compuesto. El número de oxidación se asigna de acuerdo con un conjunto de reglas estándar. Son las siguientes:
- Un átomo de un elemento puro tiene un número de oxidación de cero.
- Para los átomos individuales de un ion, su número de oxidación es igual a su carga.
- El flúor es siempre -1 en los compuestos.
- El Cl, el Br y el I son siempre -1 en compuestos, excepto cuando se combinan con O o el F.
- H es normalmente +1 y O es normalmente -2.
- El número de oxidación de un compuesto es igual a la suma de los números de oxidación de cada átomo del compuesto.
Formación de compuestos iónicos
Conocer el número de oxidación de un compuesto es muy importante cuando se habla de compuestos iónicos. Los compuestos iónicos son combinaciones de iones positivos y negativos. Generalmente se forman cuando los no metales y los metales se unen. Para determinar qué sustancia se forma, debemos utilizar las cargas de los iones implicados.
Para formar una molécula neutra, la carga positiva del catión (ión cargado positivamente) debe ser igual a la carga negativa del anión (ión cargado negativamente). Para crear una molécula cargada neutra, debe combinar los átomos en ciertas proporciones. Los científicos utilizan subíndices para identificar cuántos de cada átomo componen la molécula.
Por ejemplo, al combinar el magnesio y el nitrógeno sabemos que el ion de magnesio tiene una carga «+2» y el nitrógeno una carga «-3». Para cancelar estas cargas, debemos tener tres átomos de magnesio por cada dos átomos de nitrógeno:
El conocimiento de las cargas de los iones es crucial para conocer las fórmulas de los compuestos formados.
Los álcalis (elementos de la primera columna) forman iones «+1» como Na⁺ y Li⁺
Los metales alcalinotérreos (elementos de la 2ª columna) forman iones «2+» como el Mg²⁺ y el Ba²⁺.
Los halógenos (elementos de la séptima columna) forman iones «-1» como Cl⁻ y I⁻
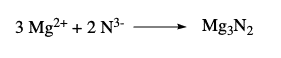
¿Cómo se nombran los compuestos iónicos?
El siguiente esquema proporciona las reglas para nombrar los compuestos iónicos:
Iones positivos
Los cationes monatómicos (un solo átomo con carga positiva) toman el nombre del elemento más la palabra «ion».
Ejemplos:
Na⁺ = ion sodio
Zn²⁺ = ion zinc
Si un elemento puede formar más de un ion positivo, la carga se indica con el número arábigo entre paréntesis al final del nombre.
Ejemplos:
Fe²⁺ = ion hierro(II)
Fe³⁺ = ion hierro (III)
Iones negativos
Los aniones monoatómicos (un solo átomo con carga negativa) en general, cambian su terminación a «-uro»
Ejemplos:
O²⁻ = ion óxido
Cl⁻ = ion cloruro
Los oxoaniones (iones poliatómicos cargados negativamente que contienen O) terminan en «-ato». Sin embargo, si hay más de un oxoanión para un elemento específico, entonces las terminaciones son:
ClO⁻: hipoclorito
ClO2⁻: clorito
ClO3⁻= clorato
ClO4⁻= perclorato
Los aniones poliatómicos (un ión cargado negativamente que contiene más de un tipo de elemento) a menudo añaden un átomo de hidrógeno; en este caso, el nombre del anión o bien añade «hidrógeno-» al principio.TABLA
Ejemplo:
CO3²⁻ se convierte en HCO³⁻
«Carbonato» se convierte en «Hidrógeno Carbonato»
Cuando se combinan cationes y aniones en un compuesto iónico, siempre se pone primero el nombre del catión y luego el del anión (las fórmulas moleculares también se escriben en este orden).
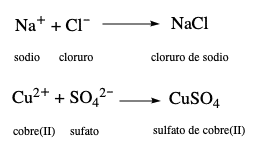
Ejemplos:
La disposición de los átomos: ¿cómo influye en la nomenclatura?
Al nombrar los iones, es importante considerar los «isómeros». Los isómeros son compuestos con la misma fórmula molecular, pero con diferentes disposiciones de átomos. Por lo tanto, es importante incluir alguna señal dentro del nombre del ion que identifique de qué disposición está hablando. Hay tres tipos principales de clasificación: isómeros geométricos, ópticos y estructurales.
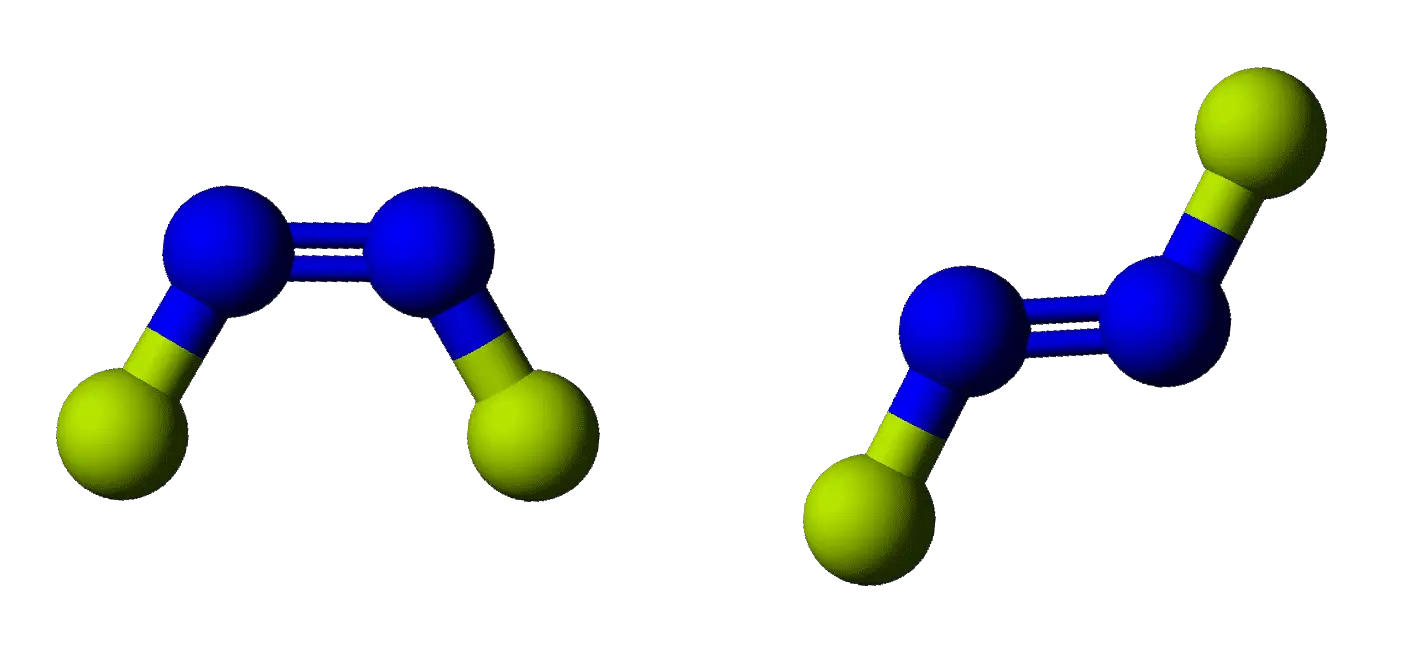
Los isómeros geométricos se refieren al lado en que se encuentran los átomos o iones. Los prefijos utilizados para distinguir los isómeros geométricos son cis, que significa que los sustituyentes se encuentran en el mismo lado del ion, y trans, que significa que se encuentran en lados opuestos.
A continuación se muestra un dibujo para ayudarte, recuerda que el isómero de la izquierda corresponde al CIS y el de la derecha al TRANS:
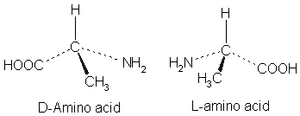
Los isómeros ópticos difieren en la disposición de cuatro grupos alrededor de un carbono quiral. Estos dos isómeros se diferencian como L y D. Y serán cada uno la imagen especular del otro.
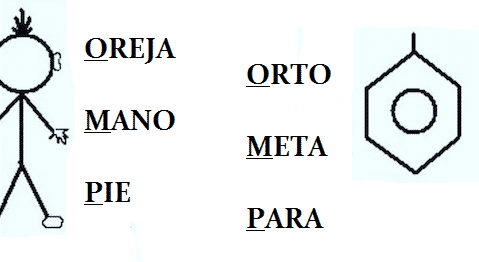
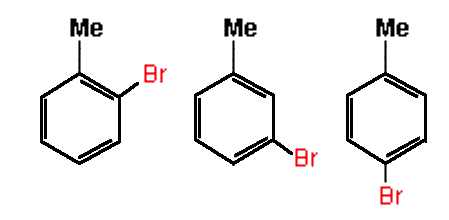
Los isómeros estructurales diferencian la colocación de dos átomos de cloro alrededor de un anillo hexagonal de carbono. Estos tres isómeros se identifican como orto, meta, y para. También le damos un pequeño dibujo de gran utilidad:
Nombrando los compuestos moleculares binarios
Los compuestos moleculares se forman a partir de la unión covalente entre elementos no metálicos. La nomenclatura de estos compuestos se describe en el siguiente conjunto de reglas:
- El átomo más positivo se escribe primero (el átomo que está más a la izquierda y al fondo de la tabla periódica)
- El segundo átomo más negativo tiene un final «-uro».
- Cada prefijo indica el número de cada átomo presente en el compuesto.
Ejemplos:
CO2 = dióxido de carbono
P4S10 = decasulfuro de tetrafósforo
Cómo nombrar a los ácidos inorgánicos
Los ácidos binarios (H + un elemento no metálico) son ácidos que se disocian en átomos de hidrógeno y aniones en el agua. Los ácidos que sólo liberan un átomo de hidrógeno se conocen como monopróticos. Los ácidos que liberan más de un átomo de hidrógeno se denominan polipróticos. Al nombrar las disoluciones acuosas de éstos ácidos binarios, simplemente se añade «ácido» (que denota la presencia de un átomo de hidrógeno) al principio y «-hídrico» al final del nombre del anión. Las combinaciones del hidrógeno con los elementos del grupo 17 se nombrarán como halogenuros de hidrógeno.
Ejemplos:
HCl = ácido clorhídrico
HBr = ácido bromhídrico
Los ácidos ternarios (también llamados oxoácidos, están formados por hidrógeno, otro elemento y oxígeno) se basan en el nombre del anión. En este caso, los sufijos -ato y -ito para el anión se sustituyen por -ico y -oso respectivamente. El nuevo nombre del anión es entonces seguido por la palabra «ácido».
Ejemplo:
ClO4⁻ a HClO4 De perclorato a ácido perclórico.
ClO⁻ a HClO => De hipoclorito a ácido hipocloroso.
¿Cómo nombrar a los compuestos químicos?
La formulación de los compuestos químicos es muy extensa, desde los compuestos binarios más sencillos hasta complejos metálicos con grados altos de coordinación, aunque todos los conceptos de nomenclatura exceden este contenido, se presentan algunos fundamentos.
Prefijo según el número de carbonos:
1 met-
2 et-
3 prop-
4 but-
5 pent-
6 hex-.
7 hept-
8 oct-
9 non-
10 dec-
Hay cuatro tipos básicos de hidrocarburos orgánicos, aquellos compuestos químicos que contienen sólo carbono e hidrógeno:
Enlaces simples (alcano): el sufijo es «ano», fórmula CnH2n+2
Doble enlace (alqueno): el sufijo es «eno», fórmula CnH2n
Triple enlace (alquino): el sufijo es «ino», fórmula CnH2n-2
Compuestos cíclicos: utilice el prefijo «ciclo».
Así, por ejemplo, un compuesto orgánico con la fórmula «C6H14» se reconocería como un alcano con seis carbonos, por lo que su nombre es «hexano».
¿TE GUSTARÍA UNIRTE A UN CURSO?
O si lo prefieres tengo estos cursos de pago en los que puedo guiarte mucho mejor.
https://www.udemy.com/course/formulacion-nomenclatura-quimica/





